Osteoporose
OSTEOPOROSE – KURZÜBERBLICK
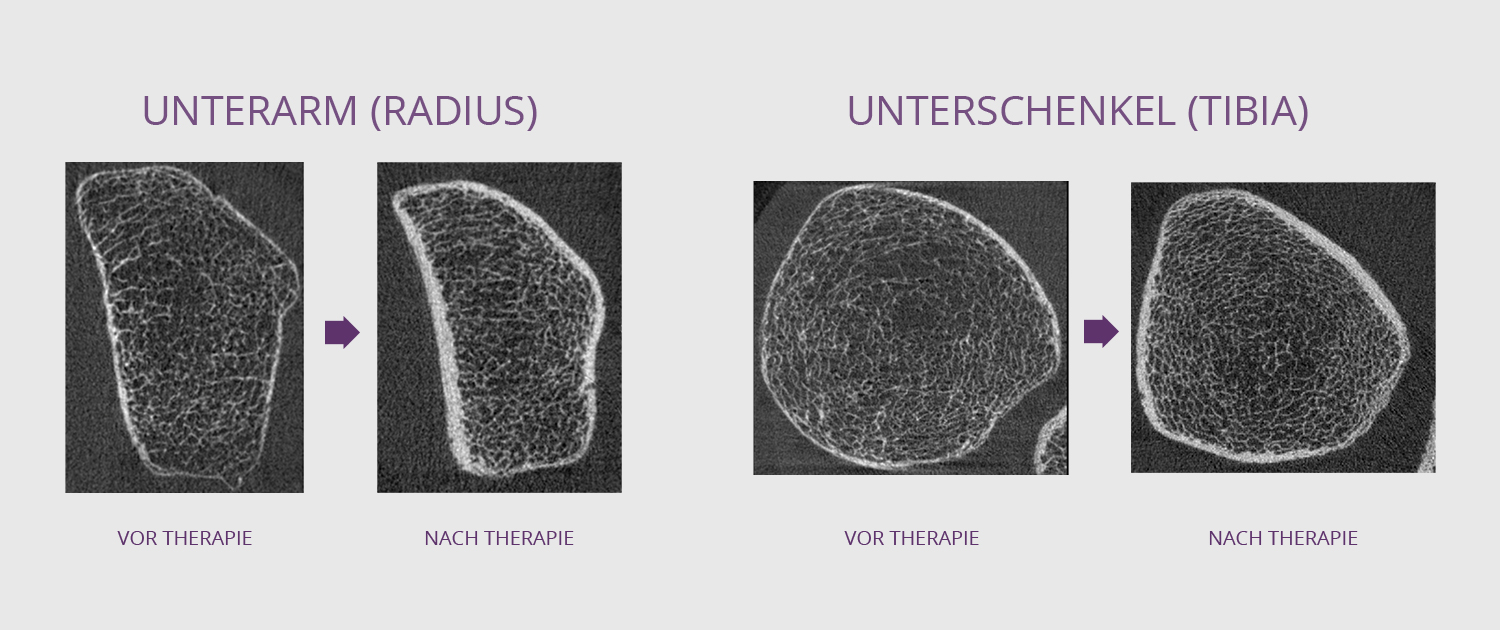
Die Knochenbrüchigkeit/-Fragilität entsteht durch das Zusammenspiel von:
- verminderter Knochenmasse
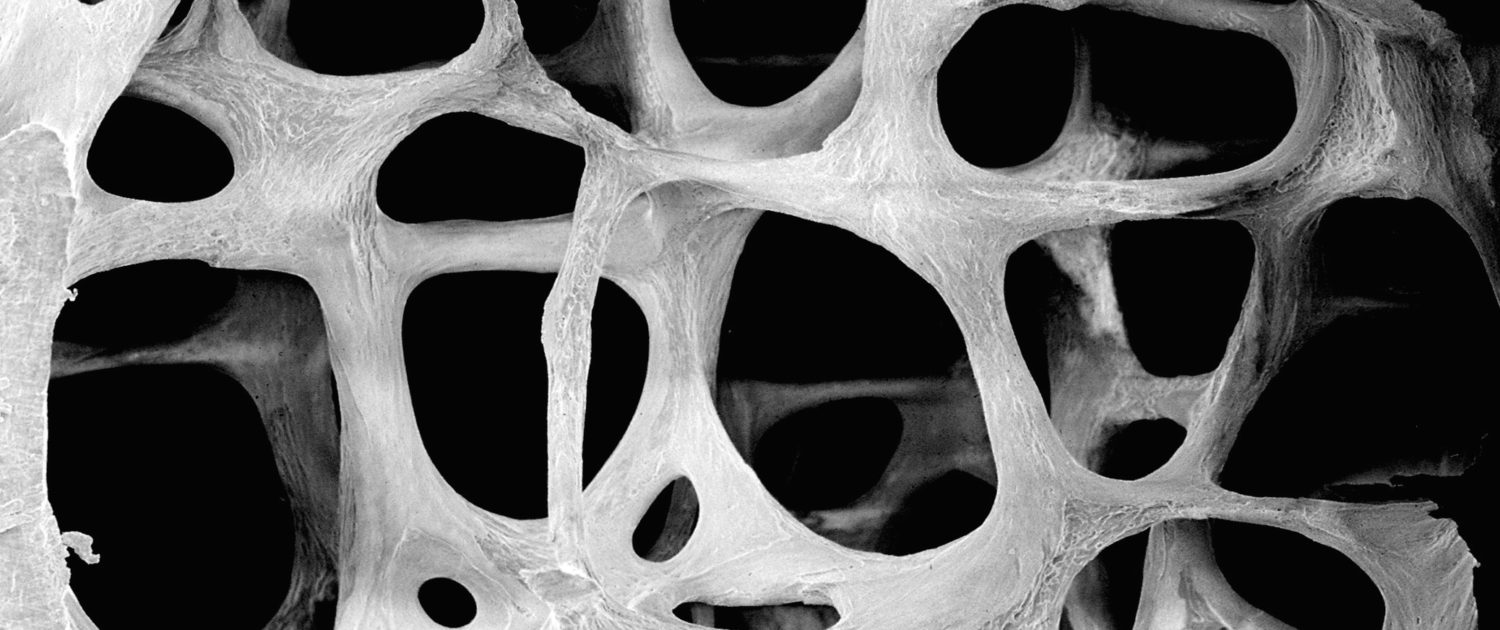
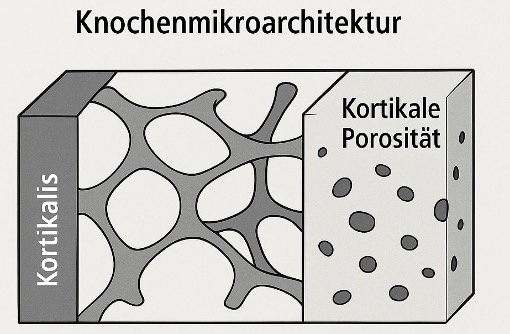
- gestörter Mikroarchitektur
- veränderter Knochengeometrie
- reduzierter Materialqualität
- gestörter Anpassung an mechanische Belastung
Eine alleinige Betrachtung der Knochendichte (BMD – DXA Messung) reicht daher nicht aus, um das Frakturrisiko zuverlässig zu erklären.
LEBENSLANGE ENTSTEHUNGSMECHANISMEN DER OSTEOPOROSE
Es werden zwei Hauptursachen wissenschaftlich diskutiert:
A) Zu geringe Knochenspitzenmasse (Peak Bone Mass)
Entsteht in Kindheit & Jugend durch:
- genetische Faktoren
- Hormonstatus
- Ernährung
- körperliche Aktivität
→ Ein niedriges Startniveau erhöht das Frakturrisiko im Alter erheblich. „Knochenerwachsen“ wird der Mensch erst Anfang/Mitte 20.
B) Übermäßiger Knochenabbau im Alter
Der Knochen wird lebenslang durch Remodeling-Einheiten (bone remodeling untis – BMUs; dort wo auch Medikamente gezielt eingreifen) umgebaut:
- Osteoklasten bauen Knochen ab
- Osteoblasten bauen wieder auf
Im Alter entsteht bei allen Menschen eine negative Bilanz → gestörtes Gleichgewicht – mehr Abbau als Anbau – entscheidet ist das Ausmaß dieses Ungleichgewichtes. Es wird mehr Knochen abgebaut als neu gebildet.
Besonders stark:
- bei Frauen nach der Menopause (Östrogenmangel) oder eine Menopause vor dem 45. Lebensjahr
- bei Männern bei Hypogonadismus (Testosteronmangel)
- bei Vitamin-D-Mangel
- Bei klinischen Risikofaktoren oder Erkrankungen bzw. Medikamente, welche das Knochenbruch Risiko erhöhen
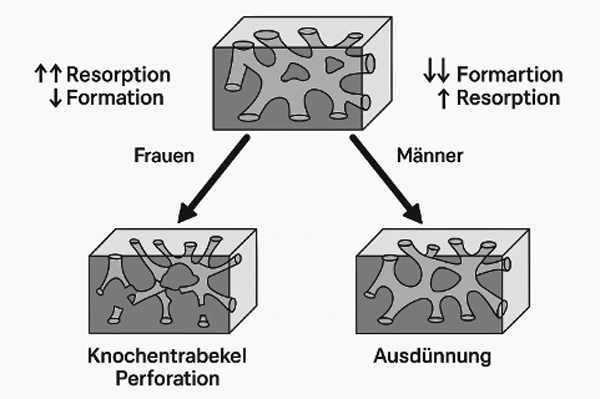
GESCHLECHTSSPEZIFISCHE UNTERSCHIEDE
Frauen:
- Nach der Menopause:
- massive Zunahme der Remodeling-Aktivität
- tiefere Resorptionslakunen
- Verlust von Trabekel-Verbindungen
- Weniger periostaler Knochenanbau. Dies bedeutet, dass der Knochen an der äußeren Begrenzung des Knochen weniger aufbaut und dadurch weniger stabil wird
Männer:
- Knochenverlust v. a. durch:
- dünner werdende Trabekel
- weniger durch vollständigen Abbau
- Stärkerer periostaler Ausgleich
→ relative Erhaltung der Biegefestigkeit
ROLLE VON ÖSTROGEN (BEI BEIDEN GESCHLECHTERN!)
Östrogen:
- hemmt Osteoklasten (Knochen abbauende Zellen)
- verkürzt ihre Lebensdauer
- fördert das Gleichgewicht zwischen Abbau und Aufbau
Sinkt es:
→ beschleunigter Knochenabbau bei Frauen und Männern.
GENETISCHE FAKTOREN
- Knochenstruktur ist stark genetisch mitbestimmt
- Aber:
- Kein einzelnes Gen erlaubt derzeit eine sichere Frakturrisiko-Vorhersage
- Genetik erklärt nur einen Teil des Risikos
- Umwelt, Bewegung, Hormone & Ernährung sowie körperliche Aktivität bleiben entscheidend
ZENTRALE SCHLUSSFOLGERUNGUNGEN
Menschen mit:
- Osteoporotischen Frakturen
- niedriger Knochendichte oder Veränderung der Knochenmikroarchitektur
- Klinischen Risikofaktoren
bilden keine einheitliche Krankheitsgruppe.
→ Eine pauschale Aussage greift daher oft zu kurz. Die individuelle Evaluation und Berechung des Knochenbruch Risikos (FRAX Berechnung – nicht nur die Knochendichte in der DXA Messung!) ist daher entsprechend der Österreichischen Behandlungs Leiltinie entscheidend für die Beurteilung eines möglicherweise erhöhten persönlichen Knochenbruch Risikos. Die FRAX Berechung ist die Grundlage für die therapeutische Empfehlung (Basismaßnahmen und eventuell zusätzlich Medikamente zur Senkung eines erhöhten Knochenbruch Risikos).
FAZIT:
Die Erkrankung Osteoporose entsteht lebenslang durch das Zusammenwirken von unzureichendem Knochenaufbau, hormonell bedingtem Knochenabbau, gestörter Mikroarchitektur und unzureichender mechanischer Anpassung – nicht allein durch eine niedrige Knochendichte.
Daher ist die FRAX Berechung des persönlichen Knochenbruch Risiko entscheidend für die Therapie einer Osteoporose.
Wichtig: Ein osteoporotischer Kncohenbruch ist immer eine absolute und vor allem langfristige Behandlunsindikation.